Az ionkötés, fémes kötés és kovalens kötés a három legfontosabb... Továbbiak megjelenítése
Regisztrálj, hogy lásd a tartalmatTeljesen ingyenes!
Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
Knowunity AI
Tantárgyak
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Összes témakör megjelenítése
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Összes témakör megjelenítése
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Összes témakör megjelenítése
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Összes témakör megjelenítése
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Összes témakör megjelenítése
203
•
Frissítve Apr 15, 2026
•
Rigó Jázmin
@rigjzmin
Az ionkötés, fémes kötés és kovalens kötés a három legfontosabb... Továbbiak megjelenítése










Az ionok töltéssel rendelkező részecskék, amelyek akkor keletkeznek, amikor az atomok elektronokat adnak le vagy vesznek fel. A kationok pozitív töltésűek (Na⁺, Ca²⁺, Al³⁺), míg az anionok negatív töltésűek (Cl⁻, O²⁻, S²⁻).
Az összetett ionok több atomból állnak, de együtt viselkednek egyetlen töltött részecskének. Ilyenek például az SO₄²⁻ (szulfát), CO₃²⁻ (karbonát), NH₄⁺ (ammónium) ionok.
Az ionvegyületek kationokból és anionokból épülnek fel úgy, hogy a pozitív és negatív töltések kiegyenlítik egymást. Példák: NaCl, CaCl₂, MgO.
Fontos: Az ionrácsban az azonos töltésű ionok a legtávolabb, az ellentétes töltésűek a legközelebb helyezkednek el egymáshoz.

Az ionkötés az ellentétes töltésű ionok közötti vonzó kölcsönhatás. Minél kisebbek az ionok és nagyobb a töltésszámuk, annál erősebb a kötés.
Az ionvegyületek magas olvadás- és forrásponttal rendelkeznek, törékények és ridegek. Szobahőmérsékleten szilárdak, de jól oldódnak vízben.
A vizes oldatban a vízmolekulák körbeveszik az ionokat - ez a hidratáció. Az oldatban szabadon mozgó ionok miatt az ionvegyületek oldatai vezetik az elektromos áramot.
Megjegyzés: Szilárd állapotban az ionvegyületek nem vezetik az áramot, csak oldat vagy olvadék állapotban.

Az ionizációs energia (Ei) megmutatja, mennyi energiára van szükség ahhoz, hogy egy atomból elektront távolítsunk el. Minél nagyobb a rendszám, annál nagyobb az ionizációs energia.
Az elektronaffinitás (Eaff) azt mutatja meg, milyen energiaváltozás történik, amikor egy atom elektront vesz fel. Ez lehet pozitív (energiát kell befektetni) vagy negatív (energia szabadul fel).
Ezek az értékek segítenek megérteni, hogy mely atomok alakulnak könnyen kationná vagy anionná. A fémek kis ionizációs energiával, a nemfémek nagy elektronaffinitással rendelkeznek.
Tipp: A periódusos rendszerben balról jobbra haladva nő az ionizációs energia, felülről lefelé csökken.

A periódusos rendszer több mint 80%-a fémes elem. Szinte mind szilárd halmazállapotú (kivéve a higany), fényesek, vezetik a hőt és az áramot.
A fémrács rácspontjaiban fématomok vannak, közöttük delokalizált elektronok mozognak. Ezek az elektronok nem egy atomhoz kötöttek, hanem szabadon vándorolnak.
A fémes kötés a pozitív fémiontörzsek és a delokalizált elektronok közötti vonzó kölcsönhatás. Ez tartja össze a fémrácsot és magyarázza a fémek különleges tulajdonságait.
Kulcsfogalom: A delokalizált elektronok miatt vezetik a fémek olyan jól az áramot és a hőt.

A fémek sűrűség alapján két csoportra oszthatók: könnyűfémek és nehézfémek .
Az olvadáspont és keménység nagyon változó: vannak puha fémek (Na, Pb), amelyeket késsel lehet vágni, és kemény fémek (W, V). A megmunkálhatóság is eltérő - az arany és ezüst kiválóan formálható.
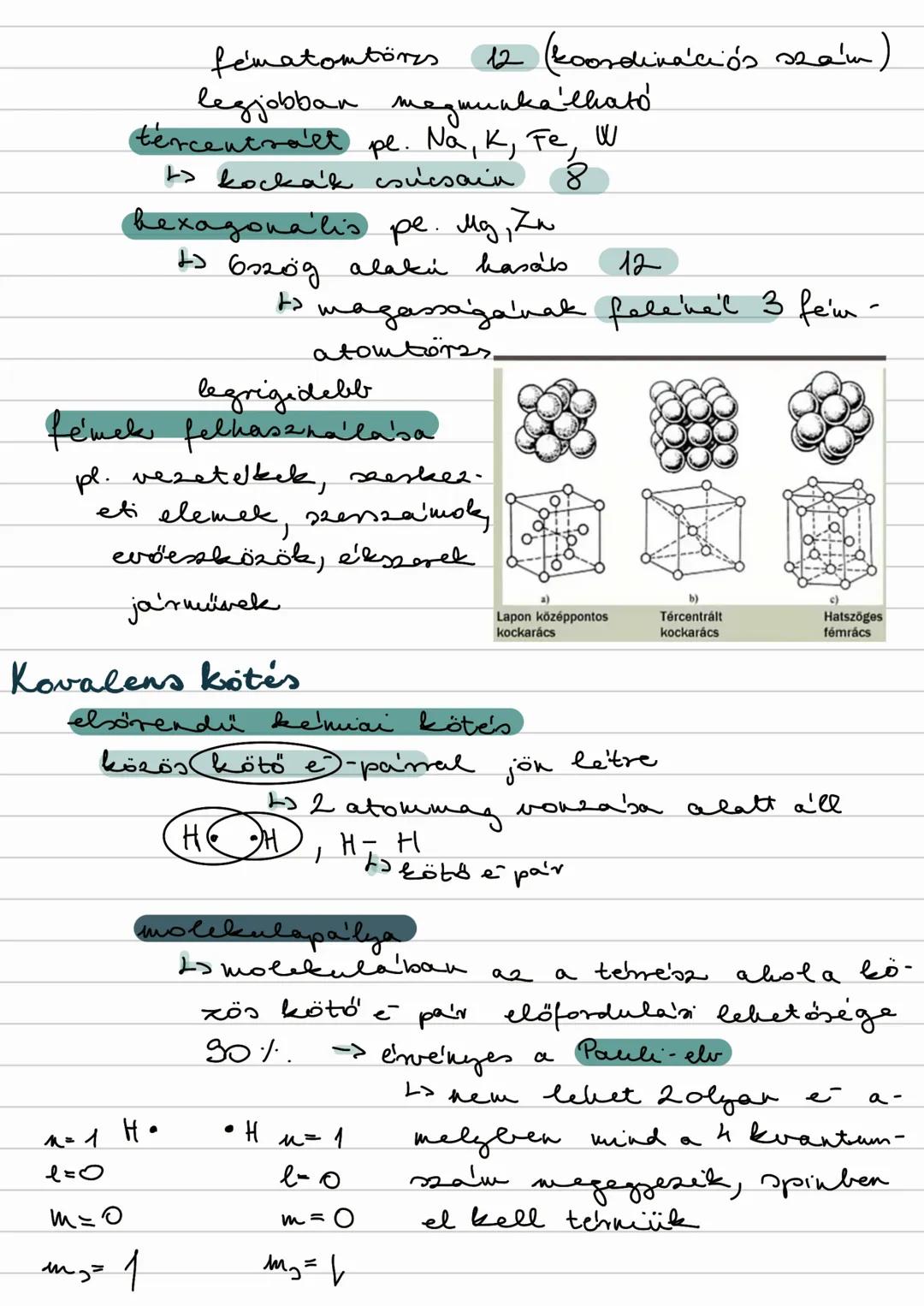
A fémrács típusa meghatározza a tulajdonságokat. A lapcentrált rácsú fémek (Au, Cu) a legjobban megmunkálhatók, a tércentrált (Fe, W) és hexagonális (Mg, Zn) rácsúak kevésbé.
Érdekes: A koordinációs szám megmutatja, hány közvetlen szomszédja van egy fématomnak a rácsban.
A kovalens kötés közös kötő elektronpár révén jön létre két atom között. Ez az elektronpár mindkét atommag vonzása alatt áll, és molekulapályán mozog.
A kötésben résztvevő elektronokra érvényes a Pauli-elv: nem lehet két olyan elektron, amelynek mind a négy kvantumszáma megegyezik. Ezért a kötő elektronpárban az elektronok spinje ellentétes.
Ez az elsőrendű kémiai kötés különösen jellemző a nemfémek között. A H-H kötés a legegyszerűbb példa erre.
Fontos: A molekulapálya az a térség, ahol a közös elektronpár 90%-os valószínűséggel megtalálható.
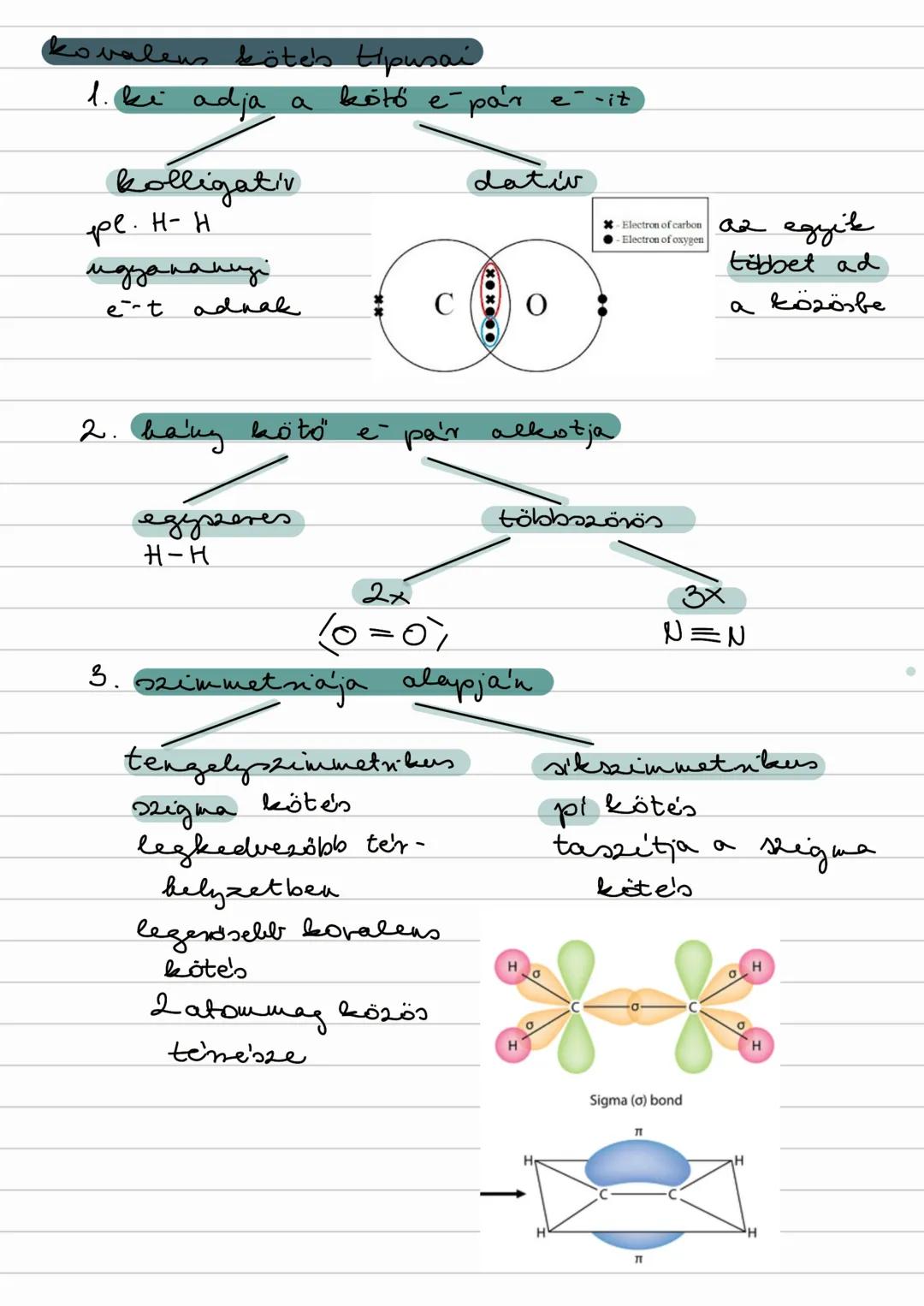
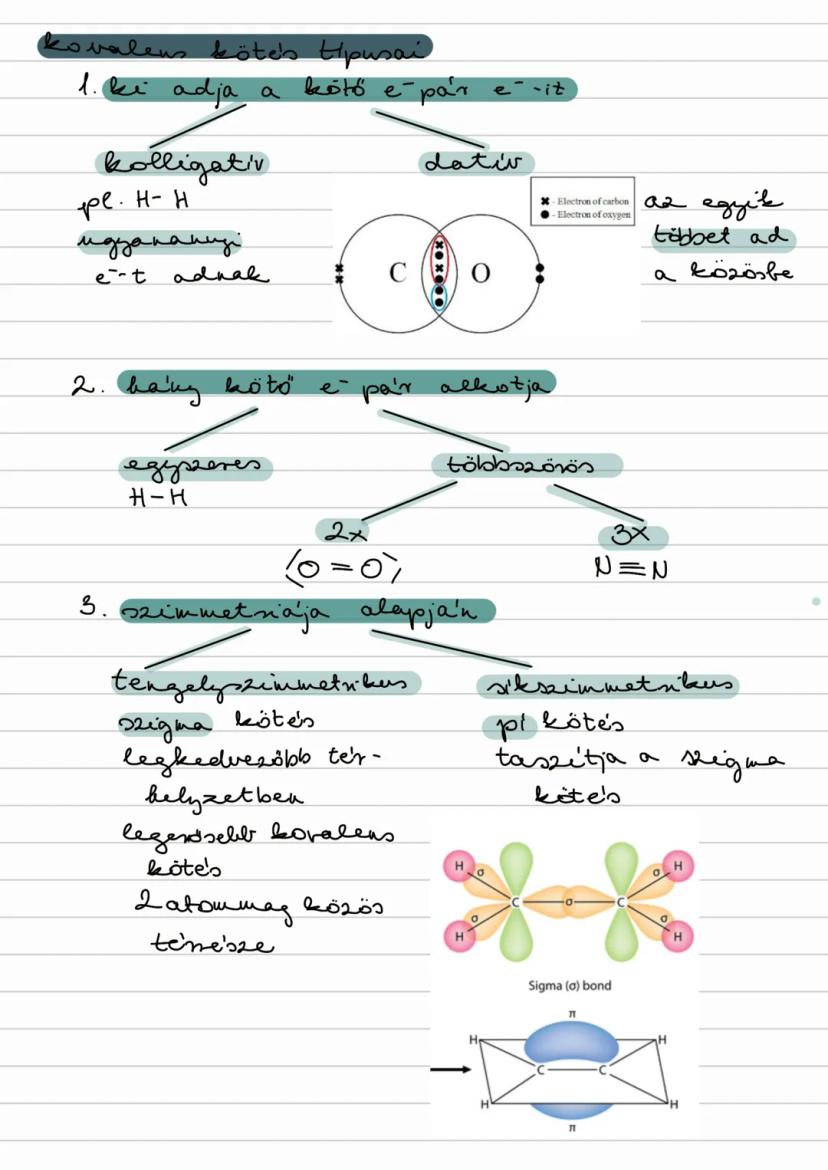
Elektronadás szerint: kolligatív és datív (egyik atom többet ad a közösbe).
Kötő elektronpárok száma szerint: egyszeres , kétszeres és háromszoros (N≡N) kötések.
Szimmetria szerint: szigma kötés (tengely szimmetrikus, legerősebb) és pi kötés (sík szimmetrikus, gyengébb).
Megjegyezni való: A többszörös kötésekben mindig van egy szigma kötés, a többi pi kötés.

Polaritás szerint: apoláris kötés azonos atomok között , poláris kötés különböző atomok között . A poláris kötésben van pozitív és negatív pólus.
Lokalizáció szerint: lokalizált kötés két atommag vonzása alatt, delokalizált kötés több atommag vonzása alatt áll.
A kötéstávolság a kapcsolódó atommagok közötti távolság, a kötési energia pedig a kötés felszakításához szükséges energia.
Atomrács: Amikor kovalens kötések háromdimenziós hálózatot alkotnak, atomrács keletkezik (pl. gyémánt).

A molekula több atomból álló semleges részecske. Lehet elemmolekula (azonos atomokból, pl. H₂, O₂) vagy vegyületmolekula (különböző atomokból).
A szerkezeti képletben látható a kötések elrendeződése. Fontos megkülönböztetni a kötő elektronpárokat (két atommag vonzása alatt) és a nemkötő elektronpárokat (egy atommag vonzása alatt).
Kétatomos molekuláknál egyszerű: ha a kötés poláris, a molekula is poláris. Ha apoláris a kötés, apoláris a molekula.
Alapszabály: Az elemmolekulák mindig apolárisak, mert azonos atomokat tartalmaznak.

Többatomos molekuláknál bonyolultabb a helyzet: figyelembe kell venni az összes kötés polaritását és a molekula alakját.
Fontos szabály: Ha a központi atomnak van nemkötő elektronpárja, a molekula általában poláris (pl. H₂O, NH₃). Ha nincs nemkötő elektronpárja, gyakran apoláris (pl. CH₄).
Példák: CO₂ lineáris alakja miatt apoláris, bár a C=O kötések polárisak. A H₂O V alakja miatt poláris.
Tipp: A molekula alakja legalább olyan fontos, mint a kötések polaritása a molekula összpolaritásának meghatározásában.
MI Társunk egy diákközpontú MI eszköz, amely többet nyújt puszta válaszoknál. Millió Knowunity erőforrásra épülve releváns információkat, személyre szabott tanulási terveket, kvízeket és tartalmat biztosít közvetlenül a chatben, alkalmazkodva az egyéni tanulási utadhoz.
Az appot letöltheted a Google Play Store-ból és az Apple App Store-ból.
Pontosan! Élvezd az ingyenes hozzáférést a tanulási tartalmakhoz, kapcsolódj diáktársaiddal, és kapj azonnali segítséget – mind a kezed ügyében.
App Store
Google Play
Az alkalmazás nagyon könnyen használható és jól megtervezett. Mindent megtaláltam, amit eddig kerestem, és sokat tudtam tanulni a prezentációkból! Biztosan használni fogom az alkalmazást egy osztályfeladathoz! És persze inspirációként is nagyszerűen segít.
Stefan S
iOS felhasználó
Ez az alkalmazás tényleg nagyszerű. Olyan sok tanulási jegyzet és segítség van benne [...]. Például a francia a problémás tantárgyam, és az alkalmazásban olyan sok segítség lehetőség van. Ennek az alkalmazásnak köszönhetően javult a franciám. Mindenkinek ajánlanám.
Samantha Klich
Android felhasználó
Hű, tényleg lenyűgözött. Csak úgy kipróbáltam az alkalmazást, mert sokszor láttam reklámozva, és teljesen megdöbbentett. Ez az alkalmazás AZ A SEGÍTSÉG, amire az iskolában szükséged van, és mindenekelőtt olyan sok mindent kínál, mint például gyakorlatokat és összefoglalókat, amik nekem személyesen NAGYON hasznosak voltak.
Anna
iOS felhasználó
A legjobb app a földön! Nincs szó rá, mert túl jó
Thomas R
iOS felhasználó
Egyszerűen elképesztő. 10x jobban tudok ismételni vele, ez az app egy egyértelmű 10/10. Mindenkinek ajánlom. Nézhetem és kereshetem a jegyzeteket. El tudom menteni őket tantárgy mappákba. Bármikor átismételhetem, amikor visszatérek. Ha még nem próbáltad ezt az appot, tényleg lemaradsz valamiről.
Basil
Android felhasználó
Ez az app sokkal magabiztosabbá tett a vizsgafelkészülésben, nem csak azáltal, hogy növelte az önbizalmam olyan funkciókkal, amik lehetővé teszik, hogy kapcsolódj másokhoz és kevésbé érezd magad egyedül, hanem azáltal is, ahogy maga az app arra épül, hogy jobban érezd magad. Könnyű navigálni, szórakoztató használni, és hasznos bárkinek, aki bármilyen területen küzd.
David K
iOS felhasználó
Az alkalmazás egyszerűen nagyszerű! Csak be kell írnom a témakört a keresősávba, és szuper gyorsan megkapom a választ. Nem kell megnéznem 10 YouTube videót, hogy megértsek valamit, így időt spórolok. Nagyon ajánlom!
Sudenaz Ocak
Android felhasználó
Az iskolában nagyon rossz voltam matekból, de az alkalmazásnak köszönhetően most jobban megy. Annyira hálás vagyok, hogy megcsináltátok az appot.
Greenlight Bonnie
Android felhasználó
nagyon megbízható app, ami segít fejleszteni a matekos, angolος és más kapcsolódó témákat a munkáidban. kérlek használd ezt az appot, ha nehézségeid vannak egyes területeken, ez az app kulcsfontosságú ehhez. bárcsak korábban írtam volna értékelést. és ingyenes is, szóval ne izgulj emiatt.
Rohan U
Android felhasználó
Tudom, hogy sok app hamis fiókokat használ az értékelések növelésére, de ez az app megérdemli az összeset. Eredetileg 4-est kaptam az angol vizsgáimon, és most 7-est kaptam. Három nappal a vizsga előttig nem is tudtam erről az appról, és NAGYON sokat segített. Kérlek tényleg bízz bennem és használd, mert biztos vagyok benne, hogy te is látni fogsz fejlődést.
Xander S
iOS felhasználó
A KVÍZEK ÉS TANULÓKÁRTYÁK ANNYIRA HASZNOSAK ÉS IMÁDOM A Knowunity MI-t. LITERÁLISAN OLYAN MINT A CHATGPT DE OKOSABB!! SEGÍTETT A SZEMPILLASPIRÁL PROBLÉMÁIMMAL IS!! VALAMINT A VALÓS TANTÁRGYAIMMAL IS! NYILVÁN 😍😁😲🤑💗✨🎀😮
Elisha
iOS felhasználó
Ez az app tényleg a legjobb. A tanulást olyan unalmasnak tartom, de ez az app annyira könnyűvé teszi az egész szervezését, aztán megkérheted az ingyenes MI-t, hogy teszteljen téged, annyira jó és könnyedén feltöltheted a saját anyagaidat. nagyon ajánlom mint aki most írom a gyakorló vizsgákat
Paul T
iOS felhasználó
Az alkalmazás nagyon könnyen használható és jól megtervezett. Mindent megtaláltam, amit eddig kerestem, és sokat tudtam tanulni a prezentációkból! Biztosan használni fogom az alkalmazást egy osztályfeladathoz! És persze inspirációként is nagyszerűen segít.
Stefan S
iOS felhasználó
Ez az alkalmazás tényleg nagyszerű. Olyan sok tanulási jegyzet és segítség van benne [...]. Például a francia a problémás tantárgyam, és az alkalmazásban olyan sok segítség lehetőség van. Ennek az alkalmazásnak köszönhetően javult a franciám. Mindenkinek ajánlanám.
Samantha Klich
Android felhasználó
Hű, tényleg lenyűgözött. Csak úgy kipróbáltam az alkalmazást, mert sokszor láttam reklámozva, és teljesen megdöbbentett. Ez az alkalmazás AZ A SEGÍTSÉG, amire az iskolában szükséged van, és mindenekelőtt olyan sok mindent kínál, mint például gyakorlatokat és összefoglalókat, amik nekem személyesen NAGYON hasznosak voltak.
Anna
iOS felhasználó
A legjobb app a földön! Nincs szó rá, mert túl jó
Thomas R
iOS felhasználó
Egyszerűen elképesztő. 10x jobban tudok ismételni vele, ez az app egy egyértelmű 10/10. Mindenkinek ajánlom. Nézhetem és kereshetem a jegyzeteket. El tudom menteni őket tantárgy mappákba. Bármikor átismételhetem, amikor visszatérek. Ha még nem próbáltad ezt az appot, tényleg lemaradsz valamiről.
Basil
Android felhasználó
Ez az app sokkal magabiztosabbá tett a vizsgafelkészülésben, nem csak azáltal, hogy növelte az önbizalmam olyan funkciókkal, amik lehetővé teszik, hogy kapcsolódj másokhoz és kevésbé érezd magad egyedül, hanem azáltal is, ahogy maga az app arra épül, hogy jobban érezd magad. Könnyű navigálni, szórakoztató használni, és hasznos bárkinek, aki bármilyen területen küzd.
David K
iOS felhasználó
Az alkalmazás egyszerűen nagyszerű! Csak be kell írnom a témakört a keresősávba, és szuper gyorsan megkapom a választ. Nem kell megnéznem 10 YouTube videót, hogy megértsek valamit, így időt spórolok. Nagyon ajánlom!
Sudenaz Ocak
Android felhasználó
Az iskolában nagyon rossz voltam matekból, de az alkalmazásnak köszönhetően most jobban megy. Annyira hálás vagyok, hogy megcsináltátok az appot.
Greenlight Bonnie
Android felhasználó
nagyon megbízható app, ami segít fejleszteni a matekos, angolος és más kapcsolódó témákat a munkáidban. kérlek használd ezt az appot, ha nehézségeid vannak egyes területeken, ez az app kulcsfontosságú ehhez. bárcsak korábban írtam volna értékelést. és ingyenes is, szóval ne izgulj emiatt.
Rohan U
Android felhasználó
Tudom, hogy sok app hamis fiókokat használ az értékelések növelésére, de ez az app megérdemli az összeset. Eredetileg 4-est kaptam az angol vizsgáimon, és most 7-est kaptam. Három nappal a vizsga előttig nem is tudtam erről az appról, és NAGYON sokat segített. Kérlek tényleg bízz bennem és használd, mert biztos vagyok benne, hogy te is látni fogsz fejlődést.
Xander S
iOS felhasználó
A KVÍZEK ÉS TANULÓKÁRTYÁK ANNYIRA HASZNOSAK ÉS IMÁDOM A Knowunity MI-t. LITERÁLISAN OLYAN MINT A CHATGPT DE OKOSABB!! SEGÍTETT A SZEMPILLASPIRÁL PROBLÉMÁIMMAL IS!! VALAMINT A VALÓS TANTÁRGYAIMMAL IS! NYILVÁN 😍😁😲🤑💗✨🎀😮
Elisha
iOS felhasználó
Ez az app tényleg a legjobb. A tanulást olyan unalmasnak tartom, de ez az app annyira könnyűvé teszi az egész szervezését, aztán megkérheted az ingyenes MI-t, hogy teszteljen téged, annyira jó és könnyedén feltöltheted a saját anyagaidat. nagyon ajánlom mint aki most írom a gyakorló vizsgákat
Paul T
iOS felhasználó
Rigó Jázmin
@rigjzmin
Az ionkötés, fémes kötés és kovalens kötés a három legfontosabb kémiai kötéstípus, amelyek meghatározzák az anyagok tulajdonságait. Ezek a kötések különböző módon tartják össze az atomokat, és mindegyik egyedi jellemzőkkel rendelkezik.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
Az ionok töltéssel rendelkező részecskék, amelyek akkor keletkeznek, amikor az atomok elektronokat adnak le vagy vesznek fel. A kationok pozitív töltésűek (Na⁺, Ca²⁺, Al³⁺), míg az anionok negatív töltésűek (Cl⁻, O²⁻, S²⁻).
Az összetett ionok több atomból állnak, de együtt viselkednek egyetlen töltött részecskének. Ilyenek például az SO₄²⁻ (szulfát), CO₃²⁻ (karbonát), NH₄⁺ (ammónium) ionok.
Az ionvegyületek kationokból és anionokból épülnek fel úgy, hogy a pozitív és negatív töltések kiegyenlítik egymást. Példák: NaCl, CaCl₂, MgO.
Fontos: Az ionrácsban az azonos töltésű ionok a legtávolabb, az ellentétes töltésűek a legközelebb helyezkednek el egymáshoz.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
Az ionkötés az ellentétes töltésű ionok közötti vonzó kölcsönhatás. Minél kisebbek az ionok és nagyobb a töltésszámuk, annál erősebb a kötés.
Az ionvegyületek magas olvadás- és forrásponttal rendelkeznek, törékények és ridegek. Szobahőmérsékleten szilárdak, de jól oldódnak vízben.
A vizes oldatban a vízmolekulák körbeveszik az ionokat - ez a hidratáció. Az oldatban szabadon mozgó ionok miatt az ionvegyületek oldatai vezetik az elektromos áramot.
Megjegyzés: Szilárd állapotban az ionvegyületek nem vezetik az áramot, csak oldat vagy olvadék állapotban.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
Az ionizációs energia (Ei) megmutatja, mennyi energiára van szükség ahhoz, hogy egy atomból elektront távolítsunk el. Minél nagyobb a rendszám, annál nagyobb az ionizációs energia.
Az elektronaffinitás (Eaff) azt mutatja meg, milyen energiaváltozás történik, amikor egy atom elektront vesz fel. Ez lehet pozitív (energiát kell befektetni) vagy negatív (energia szabadul fel).
Ezek az értékek segítenek megérteni, hogy mely atomok alakulnak könnyen kationná vagy anionná. A fémek kis ionizációs energiával, a nemfémek nagy elektronaffinitással rendelkeznek.
Tipp: A periódusos rendszerben balról jobbra haladva nő az ionizációs energia, felülről lefelé csökken.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
A periódusos rendszer több mint 80%-a fémes elem. Szinte mind szilárd halmazállapotú (kivéve a higany), fényesek, vezetik a hőt és az áramot.
A fémrács rácspontjaiban fématomok vannak, közöttük delokalizált elektronok mozognak. Ezek az elektronok nem egy atomhoz kötöttek, hanem szabadon vándorolnak.
A fémes kötés a pozitív fémiontörzsek és a delokalizált elektronok közötti vonzó kölcsönhatás. Ez tartja össze a fémrácsot és magyarázza a fémek különleges tulajdonságait.
Kulcsfogalom: A delokalizált elektronok miatt vezetik a fémek olyan jól az áramot és a hőt.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
A fémek sűrűség alapján két csoportra oszthatók: könnyűfémek és nehézfémek .
Az olvadáspont és keménység nagyon változó: vannak puha fémek (Na, Pb), amelyeket késsel lehet vágni, és kemény fémek (W, V). A megmunkálhatóság is eltérő - az arany és ezüst kiválóan formálható.
A fémrács típusa meghatározza a tulajdonságokat. A lapcentrált rácsú fémek (Au, Cu) a legjobban megmunkálhatók, a tércentrált (Fe, W) és hexagonális (Mg, Zn) rácsúak kevésbé.
Érdekes: A koordinációs szám megmutatja, hány közvetlen szomszédja van egy fématomnak a rácsban.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
A kovalens kötés közös kötő elektronpár révén jön létre két atom között. Ez az elektronpár mindkét atommag vonzása alatt áll, és molekulapályán mozog.
A kötésben résztvevő elektronokra érvényes a Pauli-elv: nem lehet két olyan elektron, amelynek mind a négy kvantumszáma megegyezik. Ezért a kötő elektronpárban az elektronok spinje ellentétes.
Ez az elsőrendű kémiai kötés különösen jellemző a nemfémek között. A H-H kötés a legegyszerűbb példa erre.
Fontos: A molekulapálya az a térség, ahol a közös elektronpár 90%-os valószínűséggel megtalálható.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
Elektronadás szerint: kolligatív és datív (egyik atom többet ad a közösbe).
Kötő elektronpárok száma szerint: egyszeres , kétszeres és háromszoros (N≡N) kötések.
Szimmetria szerint: szigma kötés (tengely szimmetrikus, legerősebb) és pi kötés (sík szimmetrikus, gyengébb).
Megjegyezni való: A többszörös kötésekben mindig van egy szigma kötés, a többi pi kötés.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
Polaritás szerint: apoláris kötés azonos atomok között , poláris kötés különböző atomok között . A poláris kötésben van pozitív és negatív pólus.
Lokalizáció szerint: lokalizált kötés két atommag vonzása alatt, delokalizált kötés több atommag vonzása alatt áll.
A kötéstávolság a kapcsolódó atommagok közötti távolság, a kötési energia pedig a kötés felszakításához szükséges energia.
Atomrács: Amikor kovalens kötések háromdimenziós hálózatot alkotnak, atomrács keletkezik (pl. gyémánt).

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
A molekula több atomból álló semleges részecske. Lehet elemmolekula (azonos atomokból, pl. H₂, O₂) vagy vegyületmolekula (különböző atomokból).
A szerkezeti képletben látható a kötések elrendeződése. Fontos megkülönböztetni a kötő elektronpárokat (két atommag vonzása alatt) és a nemkötő elektronpárokat (egy atommag vonzása alatt).
Kétatomos molekuláknál egyszerű: ha a kötés poláris, a molekula is poláris. Ha apoláris a kötés, apoláris a molekula.
Alapszabály: Az elemmolekulák mindig apolárisak, mert azonos atomokat tartalmaznak.

Hozzáférés minden dokumentumhoz
Javítsd a jegyeidet
Csatlakozz diákok millióihoz
Többatomos molekuláknál bonyolultabb a helyzet: figyelembe kell venni az összes kötés polaritását és a molekula alakját.
Fontos szabály: Ha a központi atomnak van nemkötő elektronpárja, a molekula általában poláris (pl. H₂O, NH₃). Ha nincs nemkötő elektronpárja, gyakran apoláris (pl. CH₄).
Példák: CO₂ lineáris alakja miatt apoláris, bár a C=O kötések polárisak. A H₂O V alakja miatt poláris.
Tipp: A molekula alakja legalább olyan fontos, mint a kötések polaritása a molekula összpolaritásának meghatározásában.
MI Társunk egy diákközpontú MI eszköz, amely többet nyújt puszta válaszoknál. Millió Knowunity erőforrásra épülve releváns információkat, személyre szabott tanulási terveket, kvízeket és tartalmat biztosít közvetlenül a chatben, alkalmazkodva az egyéni tanulási utadhoz.
Az appot letöltheted a Google Play Store-ból és az Apple App Store-ból.
Pontosan! Élvezd az ingyenes hozzáférést a tanulási tartalmakhoz, kapcsolódj diáktársaiddal, és kapj azonnali segítséget – mind a kezed ügyében.
2
Intelligens Eszközök ÚJ
Alakítsd át ezeket a jegyzeteket: ✓ 50+ Gyakorló Feladat ✓ Interaktív Tanulókártyák ✓ Teljes próbavizsga ✓ Esszé Vázlatok
App Store
Google Play
Az alkalmazás nagyon könnyen használható és jól megtervezett. Mindent megtaláltam, amit eddig kerestem, és sokat tudtam tanulni a prezentációkból! Biztosan használni fogom az alkalmazást egy osztályfeladathoz! És persze inspirációként is nagyszerűen segít.
Stefan S
iOS felhasználó
Ez az alkalmazás tényleg nagyszerű. Olyan sok tanulási jegyzet és segítség van benne [...]. Például a francia a problémás tantárgyam, és az alkalmazásban olyan sok segítség lehetőség van. Ennek az alkalmazásnak köszönhetően javult a franciám. Mindenkinek ajánlanám.
Samantha Klich
Android felhasználó
Hű, tényleg lenyűgözött. Csak úgy kipróbáltam az alkalmazást, mert sokszor láttam reklámozva, és teljesen megdöbbentett. Ez az alkalmazás AZ A SEGÍTSÉG, amire az iskolában szükséged van, és mindenekelőtt olyan sok mindent kínál, mint például gyakorlatokat és összefoglalókat, amik nekem személyesen NAGYON hasznosak voltak.
Anna
iOS felhasználó
A legjobb app a földön! Nincs szó rá, mert túl jó
Thomas R
iOS felhasználó
Egyszerűen elképesztő. 10x jobban tudok ismételni vele, ez az app egy egyértelmű 10/10. Mindenkinek ajánlom. Nézhetem és kereshetem a jegyzeteket. El tudom menteni őket tantárgy mappákba. Bármikor átismételhetem, amikor visszatérek. Ha még nem próbáltad ezt az appot, tényleg lemaradsz valamiről.
Basil
Android felhasználó
Ez az app sokkal magabiztosabbá tett a vizsgafelkészülésben, nem csak azáltal, hogy növelte az önbizalmam olyan funkciókkal, amik lehetővé teszik, hogy kapcsolódj másokhoz és kevésbé érezd magad egyedül, hanem azáltal is, ahogy maga az app arra épül, hogy jobban érezd magad. Könnyű navigálni, szórakoztató használni, és hasznos bárkinek, aki bármilyen területen küzd.
David K
iOS felhasználó
Az alkalmazás egyszerűen nagyszerű! Csak be kell írnom a témakört a keresősávba, és szuper gyorsan megkapom a választ. Nem kell megnéznem 10 YouTube videót, hogy megértsek valamit, így időt spórolok. Nagyon ajánlom!
Sudenaz Ocak
Android felhasználó
Az iskolában nagyon rossz voltam matekból, de az alkalmazásnak köszönhetően most jobban megy. Annyira hálás vagyok, hogy megcsináltátok az appot.
Greenlight Bonnie
Android felhasználó
nagyon megbízható app, ami segít fejleszteni a matekos, angolος és más kapcsolódó témákat a munkáidban. kérlek használd ezt az appot, ha nehézségeid vannak egyes területeken, ez az app kulcsfontosságú ehhez. bárcsak korábban írtam volna értékelést. és ingyenes is, szóval ne izgulj emiatt.
Rohan U
Android felhasználó
Tudom, hogy sok app hamis fiókokat használ az értékelések növelésére, de ez az app megérdemli az összeset. Eredetileg 4-est kaptam az angol vizsgáimon, és most 7-est kaptam. Három nappal a vizsga előttig nem is tudtam erről az appról, és NAGYON sokat segített. Kérlek tényleg bízz bennem és használd, mert biztos vagyok benne, hogy te is látni fogsz fejlődést.
Xander S
iOS felhasználó
A KVÍZEK ÉS TANULÓKÁRTYÁK ANNYIRA HASZNOSAK ÉS IMÁDOM A Knowunity MI-t. LITERÁLISAN OLYAN MINT A CHATGPT DE OKOSABB!! SEGÍTETT A SZEMPILLASPIRÁL PROBLÉMÁIMMAL IS!! VALAMINT A VALÓS TANTÁRGYAIMMAL IS! NYILVÁN 😍😁😲🤑💗✨🎀😮
Elisha
iOS felhasználó
Ez az app tényleg a legjobb. A tanulást olyan unalmasnak tartom, de ez az app annyira könnyűvé teszi az egész szervezését, aztán megkérheted az ingyenes MI-t, hogy teszteljen téged, annyira jó és könnyedén feltöltheted a saját anyagaidat. nagyon ajánlom mint aki most írom a gyakorló vizsgákat
Paul T
iOS felhasználó
Az alkalmazás nagyon könnyen használható és jól megtervezett. Mindent megtaláltam, amit eddig kerestem, és sokat tudtam tanulni a prezentációkból! Biztosan használni fogom az alkalmazást egy osztályfeladathoz! És persze inspirációként is nagyszerűen segít.
Stefan S
iOS felhasználó
Ez az alkalmazás tényleg nagyszerű. Olyan sok tanulási jegyzet és segítség van benne [...]. Például a francia a problémás tantárgyam, és az alkalmazásban olyan sok segítség lehetőség van. Ennek az alkalmazásnak köszönhetően javult a franciám. Mindenkinek ajánlanám.
Samantha Klich
Android felhasználó
Hű, tényleg lenyűgözött. Csak úgy kipróbáltam az alkalmazást, mert sokszor láttam reklámozva, és teljesen megdöbbentett. Ez az alkalmazás AZ A SEGÍTSÉG, amire az iskolában szükséged van, és mindenekelőtt olyan sok mindent kínál, mint például gyakorlatokat és összefoglalókat, amik nekem személyesen NAGYON hasznosak voltak.
Anna
iOS felhasználó
A legjobb app a földön! Nincs szó rá, mert túl jó
Thomas R
iOS felhasználó
Egyszerűen elképesztő. 10x jobban tudok ismételni vele, ez az app egy egyértelmű 10/10. Mindenkinek ajánlom. Nézhetem és kereshetem a jegyzeteket. El tudom menteni őket tantárgy mappákba. Bármikor átismételhetem, amikor visszatérek. Ha még nem próbáltad ezt az appot, tényleg lemaradsz valamiről.
Basil
Android felhasználó
Ez az app sokkal magabiztosabbá tett a vizsgafelkészülésben, nem csak azáltal, hogy növelte az önbizalmam olyan funkciókkal, amik lehetővé teszik, hogy kapcsolódj másokhoz és kevésbé érezd magad egyedül, hanem azáltal is, ahogy maga az app arra épül, hogy jobban érezd magad. Könnyű navigálni, szórakoztató használni, és hasznos bárkinek, aki bármilyen területen küzd.
David K
iOS felhasználó
Az alkalmazás egyszerűen nagyszerű! Csak be kell írnom a témakört a keresősávba, és szuper gyorsan megkapom a választ. Nem kell megnéznem 10 YouTube videót, hogy megértsek valamit, így időt spórolok. Nagyon ajánlom!
Sudenaz Ocak
Android felhasználó
Az iskolában nagyon rossz voltam matekból, de az alkalmazásnak köszönhetően most jobban megy. Annyira hálás vagyok, hogy megcsináltátok az appot.
Greenlight Bonnie
Android felhasználó
nagyon megbízható app, ami segít fejleszteni a matekos, angolος és más kapcsolódó témákat a munkáidban. kérlek használd ezt az appot, ha nehézségeid vannak egyes területeken, ez az app kulcsfontosságú ehhez. bárcsak korábban írtam volna értékelést. és ingyenes is, szóval ne izgulj emiatt.
Rohan U
Android felhasználó
Tudom, hogy sok app hamis fiókokat használ az értékelések növelésére, de ez az app megérdemli az összeset. Eredetileg 4-est kaptam az angol vizsgáimon, és most 7-est kaptam. Három nappal a vizsga előttig nem is tudtam erről az appról, és NAGYON sokat segített. Kérlek tényleg bízz bennem és használd, mert biztos vagyok benne, hogy te is látni fogsz fejlődést.
Xander S
iOS felhasználó
A KVÍZEK ÉS TANULÓKÁRTYÁK ANNYIRA HASZNOSAK ÉS IMÁDOM A Knowunity MI-t. LITERÁLISAN OLYAN MINT A CHATGPT DE OKOSABB!! SEGÍTETT A SZEMPILLASPIRÁL PROBLÉMÁIMMAL IS!! VALAMINT A VALÓS TANTÁRGYAIMMAL IS! NYILVÁN 😍😁😲🤑💗✨🎀😮
Elisha
iOS felhasználó
Ez az app tényleg a legjobb. A tanulást olyan unalmasnak tartom, de ez az app annyira könnyűvé teszi az egész szervezését, aztán megkérheted az ingyenes MI-t, hogy teszteljen téged, annyira jó és könnyedén feltöltheted a saját anyagaidat. nagyon ajánlom mint aki most írom a gyakorló vizsgákat
Paul T
iOS felhasználó